I. Visió general de laESMODirectrius 2025
L'agost de 2025, l'ESMO va publicar oficialment la Guia de pràctica clínica de l'ESMO per al diagnòstic, tractament i seguiment del càncer de pulmó no microcític precoç i localment avançat, publicada a la revista oncològica de primer nivell, Annals of Oncology. Aquesta és la primera actualització completa des de la versió del 2017 i proporciona una referència extremadament autoritària per als oncòlegs de tot el món.

El càncer de pulmó té la incidència i mortalitat més altes de totes les neoplàsies malignes a nivell mundial. Cada any, hi ha més de 2,2 milions de casos nous i més d'1,8 milions de morts, cosa que converteix el càncer de pulmó en la principal causa de mort relacionada amb el càncer tant en homes com en dones. El càncer de pulmó no microcític (NSCLC) representa aproximadament el 80-85% de tots els pacients amb càncer de pulmó. En aquest context greu, la publicació de la guia del 2025 injecta un nou impuls científic a la pràctica clínica, i l'actualització de les estratègies de proves de biomarcadors és particularment crítica.
II. Interpretació de les principals actualitzacions de les directrius
2.1 Proves de biomarcadors: de "opcionals" a "essencials"
La guia del 2025 fa un ajust estratègic important pel que fa a les proves de biomarcadors. La guia estableix explícitament que les proves de biomarcadors són essencials per a la decisió de tractament en pacients amb NSCLC en estadi IB-III.
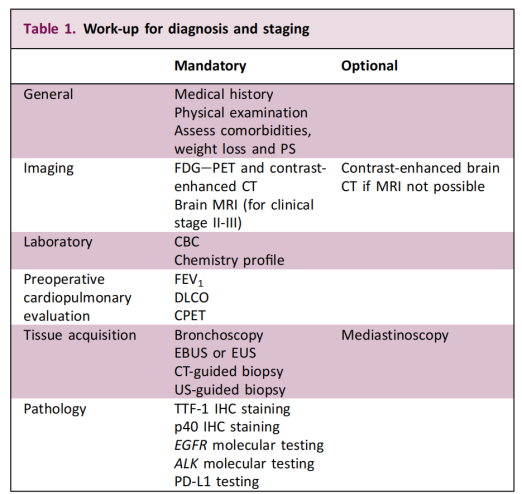
Aquesta recomanació estén les proves moleculars des del seu enfocament anterior en pacients amb malaltia avançada fins a casos resecables en fase inicial. L'objectiu principal és identificar mutacions genètiques impulsores i proporcionar una base científica per a un tractament de precisió personalitzat. La guia també emfatitza que la viabilitat de la biòpsia i l'enfocament diagnòstic han de ser determinats per un equip multidisciplinari en funció de les característiques del pacient i del tumor.
Pel que fa a l'estratègia específica de proves, la guia recomana clarament que les proves genètiques es realitzin abans de la presa de decisions quirúrgiques, i que com a mínim hagin de cobrir l'EGFR i l'ALK. Aquest concepte de "proves inicials" té una profunda importància clínica per a l'estratificació precisa i el tractament personalitzat del NSCLC en estadi inicial: la puntualitat i la precisió dels resultats de les proves determinen directament l'elecció de la teràpia adjuvant posterior.
2.2 Avenços terapèutics en el NSCLC en fase inicial positiu per a oncogens driver
La guia del 2025 integra evidència de múltiples estudis clínics importants per establir una via de tractament de precisió clara per a pacients amb NSCLC en estadi inicial positiu per a l'oncogen del conductor.
Pacients amb mutació positiva de l'EGFR:Basant-se en l'assaig ADAURA, l'osimertinib adjuvant postoperatori durant tres anys s'ha convertit en l'estàndard mundial d'atenció per a pacients amb delecions de l'exó 19 de l'EGFR o mutacions de l'exó 21 L858R. L'assaig ADAURA és un estudi internacional, multicèntric, aleatoritzat i controlat de fase III que avalua l'eficàcia i la seguretat de l'osimertinib adjuvant en pacients amb NSCLC amb mutació de l'EGFR en estadi IB-IIIA completament resectat. L'estudi va mostrar que l'osimertinib va millorar significativament tant la supervivència lliure de malaltia com la supervivència global en comparació amb el placebo, establint l'osimertinib com el nou estàndard d'atenció per a aquesta població. No obstant això, les anàlisis exploratòries de l'assaig ADAURA van indicar que aproximadament el 36% de les interrupcions precoços del tractament van ser degudes a esdeveniments adversos, i un altre 31% va ser degut a la decisió del pacient. Aquesta troballa destaca la necessitat de proves basals precises abans del tractament per garantir que s'administri una teràpia dirigida als pacients que poden obtenir un benefici sostingut.
Pacients ALK positius:Segons l'assaig ALINA, l'alectinib adjuvant postoperatori durant dos anys és ara l'estàndard de cura. En l'anàlisi primària de l'assaig ALINA aleatoritzat i obert de fase III, l'alectinib va mostrar un benefici marcat en la supervivència lliure de malaltia en la població en estadi II-IIIA, amb una raó de risc de 0,24. Les dades actualitzades de l'assaig ALINA presentades al congrés ESMO 2025 van mostrar que després de ≥3 anys de seguiment, el benefici de la supervivència lliure de malaltia (SLE) de l'alectinib es va mantenir "sostingut i clínicament significatiu", amb una raó de risc de 0,36 en la població en estadi II-IIIA. La taxa de supervivència global a 4 anys més recentment reportada va arribar al 98,4%, la taxa de SLE a 4 anys va ser del 75,5% i la SLE del sistema nerviós central també va millorar, sense nous senyals de seguretat. Aquestes dades robustes estableixen encara més l'alectinib adjuvant com l'estàndard de cura després de la resecció del NSCLC ALK-positiu i subratllen el valor de les proves precises per identificar aquests pacients.
Elecció del mètode de prova:La guia de l'ESMO del 2025 enumera explícitamentassaigs de panell de RT-PCR multiplexjuntament amb la NGS, la IHC i la FISH basades en ARN com un dels enfocaments tècnics recomanats per a la detecció de la fusió d'ALK. Això indica que el requisit principal de la guia és realitzar proves per guiar les decisions clíniques, en lloc d'exigir una plataforma de proves específica. Per als productes de RT-PCR centrats en la detecció d'EGFR i ALK, aquesta estratègia de proves flexible proporciona una justificació sòlida basada en guies per al seu ús en la pràctica clínica.
III. Solucions tècniques de proves de precisió
La guia del 2025 avança les proves a la fase de presa de decisions prequirúrgiques, cosa que eleva el llistó de la precisió, la sensibilitat i l'accessibilitat de l'assaig. Els dos productes de detecció basats en RT-PCR que es descriuen a continuació s'alineen precisament amb els requisits de la guia des d'una perspectiva tècnica.
Kit de detecció de mutacions EGFR 3.1: plataforma tecnològica ARMS millorada
Tecnologia bàsicaLa tecnologia ARMS millorada permet l'amplificació específica de seqüències mutants de baixa abundància contra un fons de tipus salvatge elevat.
Tres garanties tècniques:
-ARMS millorat → millora el reconeixement de mutacions
-Enriquiment enzimàtic → digereix el fons de tipus salvatge i enriqueix les seqüències mutants
-Bloqueig de temperatura → suprimeix l'amplificació inespecífica
RendimentSensibilitat de1% de freqüència d'al·lels mutants
Control de la contaminacióControl intern integrat + enzim UNG que evita la contaminació
Temps de respostaFuncionament de tub tancat, aproximadament120 minuts
Compatibilitat de mostres:teixit/biòpsia líquidamostres → aborda el requisit de "proves prèvies"
Cobertura:45 mutacionsen els exons 18-21 de l'EGFR, que coincideixen amb precisió amb les regions ressaltades per les directrius (delecions de l'exó 19 i l'exó 21 L858R)
Ús clínicGuia directament la teràpia amb TKI de l'EGFR
Kit de detecció de fusió EML4-ALK 3.2 MMT: solució de detecció de fusió basada en ARN

-Plataforma tecnològicaRT-PCR basada en ARN: ofereix avantatges inherents respecte als mètodes basats en ADN per a la detecció de fusions
-Avantatge basat en l'ARNDetecta directament les transcripcions de fusió expressades, evitant eficaçment els falsos negatius
-Evidència de l'estudiEn fusions d'ALK de baixa abundància, la RT-PCR és significativament més fiable que les proves basades en ADN
-SensibilitatDetecta fusions fins a20 còpies per reacció
-Cobertura de variants: Cobertes12 variants comunes de fusió EML4-ALK(inclosa la variant 1 ~33%; variants 3a/3b juntes ~29%)
-Operació i control de contaminacióTub tancat, ~120 minuts; controls de procés integrats + enzim UNG que eviten resultats falsos
-Compatibilitat d'instrumentsCompatible amb diversos instruments de PCR en temps real convencionals
-Alineació de la guiaMolt coherent amb la guia de l'ESMO
IV. Coherència entre els assaigs i les recomanacions de la guia
Els dos productes de detecció són altament coherents amb la guia ESMO 2025 de càncer de pulmó no microcític precoç i localment avançat en les dimensions clau següents:
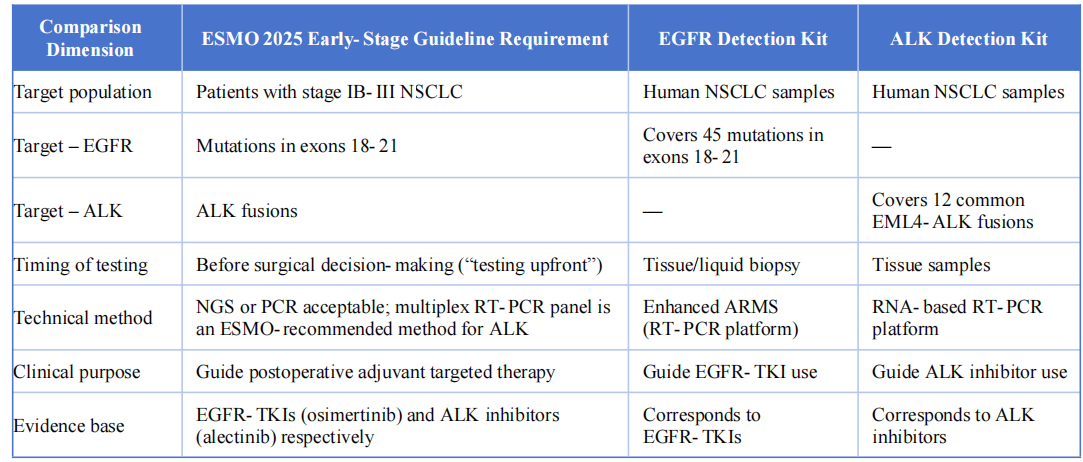
V. Conclusió
La guia ESMO 2025 per al NSCLC en fase inicial marca el començament d'una nova era de diagnòstic i tractament de precisió, centrada en "proves prèvies, orientació precisa i optimització del tractament.El kit de detecció de mutacions de l'EGFR i el kit de detecció de fusió MMT EML4-ALK compleixen els requisits de la guia pel que fa a objectius, temps i precisió a través de camins tècnics diferents.
El kit EGFR utilitza tecnologia ARMS millorada per a la detecció d'alta sensibilitat de mutacions dirigides en mostres limitades, admetent tant biòpsia de teixits com líquida per permetre "proves anticipades".
El kit ALK es basa en RT-PCR basada en ARN, oferint avantatges sobre els mètodes d'ADN per a la detecció de fusió, en línia amb la recomanació de l'ESMO de panells de RT-PCR multiplex per a les proves d'ALK.
Junts, aquests dos productes formen una solució de proves de precisió que compleix amb la guia ESMO 2025, que dóna suport a la teràpia adjuvant personalitzada per al NSCLC en fase inicial.
Referències:
- Zer A, Ahn MJ, Barlesi F, et al. Càncer de pulmó no microcític precoç i localment avançat: Guia de pràctica clínica de l'ESMO per al diagnòstic, tractament i seguiment. Ann Oncol. 2025;36(11):1245-1262. doi:10.1016/j.annonc.2025.08.003
Data de publicació: 06 de maig de 2026

