El 24 de març de 2026 es commemora el 31è Dia Mundial de la Tuberculosi. L'Organització Mundial de la Salut (OMS) ha anunciat el tema mundial d'enguany com«Sí! Podem acabar amb la tuberculosi!», emfatitzant que un fort lideratge governamental, un compromís polític sostingut i una acció multisectorial coordinada són essencials per posar fi a l'epidèmia de tuberculosi (TB).

Progrés global i reptes pendents
Segons l'Informe mundial sobre la tuberculosi 2025, el control mundial de la tuberculosi va assolir una fita important el 2024, ambincidència i mortalitat en descensper primera vegada des de la pandèmia de la COVID-19.
Un estimat10,7 milions de personesvan desenvolupar tuberculosi el 2024, incloent-hi un 54% d'homes, un 35% de dones i un 11% de nens i adolescents. Entre aquests casos, aproximadament619.000 (5,8%)estaven coinfectats amb el VIH i390.000 (3,6%)eren tuberculosi multirresistent o resistent a la rifampicina (TB MDR/RR).
La tuberculosi va causar aproximadament1,23 milions de mortsel 2024, continuant sent la principal causa infecciosa de mort a nivell mundial, superant la COVID-19. Després de tres anys d'augments entre el 2021 i el 2023, la incidència mundial de la tuberculosi va disminuir gairebé un 2% el 2024, reflectint una recuperació gradual dels serveis contra la tuberculosi.[1]
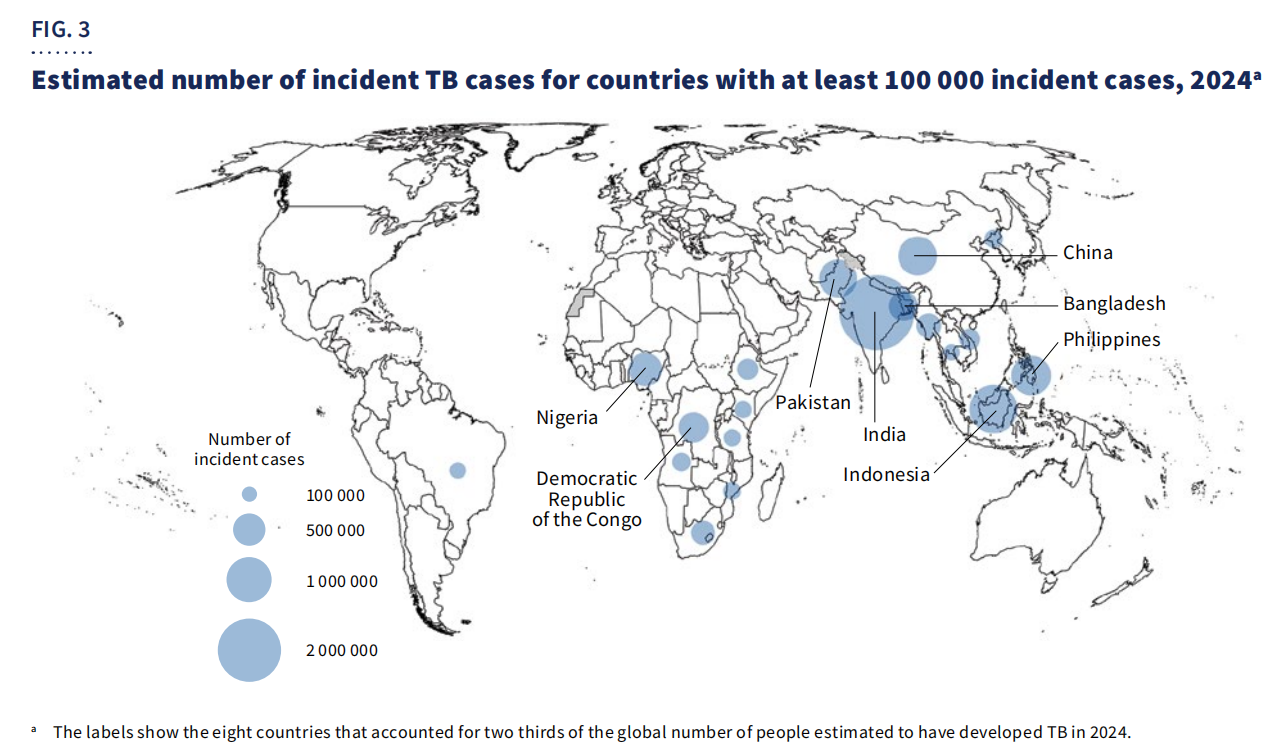
Geogràficament,67% dels casoses van concentrar en vuit països: Índia, Indonèsia, Filipines, Xina, Pakistan, Nigèria, República Democràtica del Congo i Bangladesh.
Malgrat els progressos, la tuberculosi continua sent una de les principals causes de mort entre les persones que viuen amb el VIH i un dels principals contribuents a la mortalitat associada a la resistència antimicrobiana. El finançament mundial continua sent insuficient, amb només5.900 milions de dòlars americansdisponible el 2024, molt per sota delObjectiu anual de 22.000 milions de dòlarsfixat per al 2027.
Aquestes xifres destaquen la necessitat urgent d'enfortir els programes de control de la tuberculosi a nivell mundial, amb un enfocament en l'ampliació de l'accés als diagnòstics, la millora dels resultats del tractament i l'abordatge dels determinants socials que impulsen la transmissió de la tuberculosi. La tuberculosi continua requerint una sòlida cooperació internacional i un compromís polític per assolir els objectius de l'Estratègia per acabar amb la tuberculosi.
Mycobacterium tuberculosis: Patogènesi i classificació
Mycobacterium tuberculosis (MTB/M. tuberculosis) és el patogen principal i més comú responsable de la tuberculosi (TB). Pot entrar al cos humà a través del tracte respiratori, el tracte digestiu o la pell i les membranes mucoses danyades, infectant múltiples òrgans i causant diferents formes de tuberculosi. La tuberculosi pulmonar, transmesa principalment a través de gotetes, representa més del 80% dels casos de tuberculosi. Els símptomes comuns inclouen tos, producció d'esputs i hemoptisi. Després d'una infecció als pulmons, el bacteri es pot propagar pel torrent sanguini a múltiples sistemes, cosa que pot provocar tuberculosi esquelètica, urinària o gastrointestinal.[2]
La MTB forma part del gènere Mycobacterium, que inclou:
- Complex Mycobacterium tuberculosis (MTBC): Comprèn M. tuberculosis, M. bovis, M. africanum, M. canettii i M. microti, entre d'altres. Tot i que M. tuberculosis és la causa principal de la tuberculosi, M. bovis i M. africanum també poden induir la malaltia.
- Micobacteris no tuberculosos (NTM).
- Mycobacterium leprae, la causa de la lepra.
Enfocaments de diagnòstic de laboratori
Un diagnòstic precís i oportú és essencial per a un control eficaç de la tuberculosi. L'Organització Mundial de la Salut emfatitza queLes tecnologies de diagnòstic molecular ràpid han transformat fonamentalment la detecció de la tuberculosi permetent una identificació altament sensible i específica de patògens alhora que detecta la resistència als fàrmacs.[1].
- Microscòpia i Cultiue: El cultiu continua sent el patró d'or per al diagnòstic de la tuberculosi, ja que permet la identificació definitiva d'organismes viables i dóna suport a les proves de susceptibilitat als fàrmacs i a l'anàlisi genòmica. Tanmateix, a causa de la lenta taxa de creixement de Mycobacterium tuberculosis, els resultats solen requerir de 2 a 8 setmanes, cosa que limita la seva utilitat clínica en la presa de decisions urgents.
-Proves immunològiques: Els mètodes immunològics, com ara la prova cutània de la tuberculina (TST) i els assaigs d'alliberament d'interferó gamma (IGRA), detecten les respostes immunitàries de l'hoste a la infecció per tuberculosi. Tot i que són útils per identificar infeccions latents, aquests assaigs no poden distingir de manera fiable entre la infecció activa i la prèvia i, per tant, tenen una especificitat diagnòstica limitada en entorns d'alta càrrega.
-Diagnòstic Molecular (NAAT): Es recomanen proves basades en ADN com l'amplificació d'àcids nucleics (NAAT) per la seva alta sensibilitat i especificitat.
-Seqüenciació de nova generació dirigida (tNGS): Les tecnologies de seqüenciació dirigida proporcionen una identificació d'alta resolució de mutacions associades a la resistència. Les directrius de l'OMS recomanen la tNGS com a eina avançada per a la detecció de resistència a fàrmacs posterior al diagnòstic, donant suport a estratègies de tractament de precisió [3].
-Seqüenciació metagenòmica de nova generació (mNGS): La seqüenciació metagenòmica permet la detecció imparcial d'una àmplia gamma de patògens sense selecció prèvia de la diana. Aquest enfocament és particularment valuós en escenaris clínics complexos o poc clars, com ara infeccions mixtes i pacients immunodeprimits, on els diagnòstics convencionals poden ser insuficients.
L'OMS destaca a més que la confirmació microbiològica és essencial per iniciar una teràpia adequada i millorar els resultats dels pacients, cosa que reforça la importància d'integrar el diagnòstic molecular avançat en els programes de control de la tuberculosi [1].
Solucions integrals de diagnòstic molecular de macro i micro-proves
1.Detecció de PCR multiplex per a la tuberculosi i la resistència als fàrmacsTuberculosi
| Codi de producte | Nom del producte | Certificació |
| HWTS-RT001 | Kit de detecció d'ADN de Mycobacterium Tuberculosis (PCR de fluorescència) | CE |
| HWTS-RT137 | Kit de detecció de mutacions de resistència a la isoniazida de Mycobacterium Tuberculosis (corba de fusió) | CE |
| HWTS-RT074 | Kit de detecció de resistència a l'àcid nucleic i la rifampicina de Mycobacterium Tuberculosis (corba de fusió) | CE |
| HWTS-RT102 | Kit de detecció d'àcids nucleics basat en l'amplificació isotèrmica de sondes enzimàtiques (EPIA) per a Mycobacterium tuberculosis | CE |
| HWTS-RT144 | Kit de detecció d'àcids nucleics del complex Mycobacterium Tuberculosis liofilitzat (amplificació isotèrmica amb sonda enzimàtica) | CE |
| HWTS-RT105 | Kit de detecció d'ADN de Mycobacterium Tuberculosis liofilitzat (PCR de fluorescència) | CE |
| HWTS-RT147 | Kit de detecció de resistència a la isoniazida i l'àcid nucleic de Mycobacterium Tuberculosis (corba de fusió) | CE |
Quan hi ha una forta sospita clínica de tuberculosi (TB), elHWTS-RT147Es recomana la prova per a la detecció qualitativa de la infecció per MTB i la tuberculosi multirresistent (MDR-TB). Aquesta prova identifica mutacions en elgen rpoB, que provoquen resistència a la rifampicina (RIF) i mutacions en elgens katG i InhA, que s'associen amb la resistència a la isoniazida (INH). Proporciona una prova eficient i única tant per a la MTB com per a la MDR-TB, i incorpora control de qualitat intern per minimitzar els resultats falsos negatius, garantint resultats ràpids i precisos.
2.Seqüenciació dirigida de PTNseq per a patògens respiratoris i perfils de resistència
| Codi de producte | Nom del producte | Espec. |
| HWKF-TS0001 | Kit d'enriquiment de gens de patògens d'infeccions del torrent sanguini PTNseq | 24 proves/kit |
| HWKF-TS0002 | Kit d'enriquiment genètic de microorganismes patògens per a infeccions del sistema nerviós central PTNseq | 24 proves/kit |
| HWKF-TS0003 | Kit d'enriquiment de gens de patògens d'infeccions respiratòries PTNseq | 24 proves/kit |
| HWKF-AT0003 | Kit de construcció de biblioteques d'enriquiment automatitzat per a microorganismes patògens d'infeccions respiratòries PTNseq (ONT) | 24 proves/kit |
| HWKF-TS0004 | Kit d'enriquiment gènic de patògens infecciosos d'ampli espectre PTNseq | 24 proves/kit |
| HWKF-TS0005 | Kit d'enriquiment genètic de microorganismes patògens infecciosos d'espectre ultraampli PTNseq | 24 proves/kit |
| HWKF-TS0151 | Kit d'enriquiment gènic de resistència a fàrmacs i tipificació de micobacteris (mètode d'amplificació múltiple) | 24 proves/kit |
En casos d'infeccions respiratòries mixtes (incloses infeccions de les vies respiratòries superiors i inferiors, tuberculosi i malalties respiratòries cròniques), o quan calgui una anàlisi de gens de resistència a fàrmacs (per exemple, sospita de tuberculosi resistent a fàrmacs), elSèrie PTNseq de detecció de gens d'alt rendiment dirigitses pot aplicar. Basat en tecnologia avançada de seqüenciació dirigida, PTNseq utilitza PCR ultra-multiplex per enriquir seqüències diana específiques, combinada amb seqüenciació d'alt rendiment i tecnologia de nanoporus de tercera generació per a la identificació completa de patògens i la perfilació de resistència als fàrmacs.
El sistema utilitza encebadors patentats d'alta especificitat per a l'amplificació ultramultiplex de gens diana. Amb el suport d'una base de dades patentada i algoritmes bioinformàtics intel·ligents, proporciona una identificació precisa de patògens juntament amb l'anàlisi de gens de resistència als fàrmacs i virulència. L'enriquiment dirigit redueix la interferència de l'ADN hoste, millorant la sensibilitat en mostres amb un alt fons humà i permetent la detecció eficaç d'objectius difícils com araMycobacterium tuberculosis, fongs, bacteris intracel·lulars, virus d'ARN i gens de resistència o virulència.
PTNseq arriba a un límit de detecciótan baix com 100 còpies/mli cobertes175 patògens respiratoris comuns, incloent-hi 76 bacteris, 73 virus, 19 fongs, 7 micoplasmes, així comClamídia, Rickettsiai 54 gens de resistència a fàrmacsEl panell inclou elMycobacterium tuberculosisMicobacteris no tuberculosos complexos i importants.
La sèrie PTNseq combina una alta sensibilitat amb una rendibilitat, millorant les taxes de detecció de patògens i donant suport a la teràpia antimicrobiana individualitzada, alhora que ajuda a mitigar la resistència antimicrobiana. Integrada amb el sistema de preparació de biblioteques de seqüenciació gènica (AIOS) totalment automatitzat, proporciona una solució hospitalària simplificada amb un temps de resposta de tan sols 6,5 hores des de la mostra fins al resultat.

3. Seqüenciació metagenòmica per a la detecció de patògens d'ampli espectre
| Codi de producte | Nom del producte | Espec. |
| HWKF-MN0011 | Kit de detecció de patògens metagenòmics (DNA-Illumina) | 24 proves/kit |
| HWKF-MN0018 | Kit de detecció de patògens metagenòmics (DNA-MGI) | 24 proves/kit |
| HWKF-MN0021 | Kit de detecció de patògens metagenòmics (DNA-ONT) | 24 proves/kit |
| HWKF-MN0012 | Kit de detecció de patògens metagenòmics (RNA-Illumina) | 24 proves/kit |
| HWKF-MN0019 | Kit de detecció de patògens metagenòmics (RNA-MGI) | 24 proves/kit |
| HWKF-MN0022 | Kit de detecció de patògens metagenòmics (RNA-ONT) | 24 proves/kit |
| HWKF-MN0013 | Kit de detecció de patògens metagenòmics (ADN+ARN-Illumina) | 24 proves/kit |
| HWKF-AYM0013 | Kit de construcció automatitzada de biblioteques de detecció de patògens metagenòmics (ADN+ARN-Illumina) | 24 proves/kit |
| HWKF-MN0020 | Kit de detecció de patògens metagenòmics (ADN+ARN-MGI) | 24 proves/kit |
| HWKF-MN0023 | Kit de detecció de patògens metagenòmics (ADN+ARN-ONT) | 24 proves/kit |
Quan el diagnòstic clínic no és clar,Detecció de gens d'alt rendiment de patògens mNGSes pot realitzar en diverses mostres del pacient, incloent-hi líquid de rentat broncoalveolar, esput, hisops de gola, sang, vessament pleural, pus i mostres de teixit. Aquest enfocament utilitza tecnologia de seqüenciació metagenòmica, on diferents mostres se sotmeten a un pretractament específic seguit d'una extracció d'àcids nucleics mitjançant perles de vidre i enzims de digestió de la paret, millorant l'eficiència de l'extracció. La seqüenciació s'adapta a múltiples plataformes, garantint un alt volum de dades per millorar la sensibilitat de mNGS i la integritat de l'assemblatge. Les dades s'analitzen mitjançant una base de dades autoconstruïda i algoritmes intel·ligents per detectarmés de 20.000 patògens, incloent-hi bacteris, fongs, virus i paràsits, proporcionant informació sobre microorganismes patògens sospitosos. Aquest mètode és adequat per a pacients difícils de diagnosticar, greument malalts o immunodeprimits, inclosa la identificació deBTTcomplexiNTM, així com infeccions mixtes. Millora significativament les taxes de detecció de patògens i ajuda a guiar l'ús clínic dirigit d'antibiòtics, permetent un diagnòstic precís de la infecció.
Conclusió
Tot i que s'han aconseguit progressos substancials, la tuberculosi continua sent un repte important per a la salut mundial, especialment en el context de la resistència als fàrmacs, les mancances de finançament i l'accés desigual als diagnòstics.
L'OMS emfatitza que ampliar l'accés a diagnòstics moleculars ràpids i tecnologies de seqüenciació avançades és essencial per assolir els objectius de l'Estratègia per acabar amb la tuberculosi. Amb la innovació, la inversió i la col·laboració mundial contínues, acabar amb la tuberculosi ja no és una aspiració, sinó un objectiu assolible.
Referències:
- Organització Mundial de la Salut. Informe sobre la tuberculosi mundial 2024/2025: proves diagnòstiques i tractament.
- Organització Mundial de la Salut. Manual de l'OMS per a la selecció de proves de diagnòstic ràpid moleculars recomanades per l'OMS per a la detecció de la tuberculosi i la tuberculosi resistent als fàrmacs.
- Organització Mundial de la Salut. Directrius consolidades de l'OMS sobre la tuberculosi: Mòdul 3 – Diagnòstic (actualització de 2024).
Data de publicació: 24 de març de 2026
